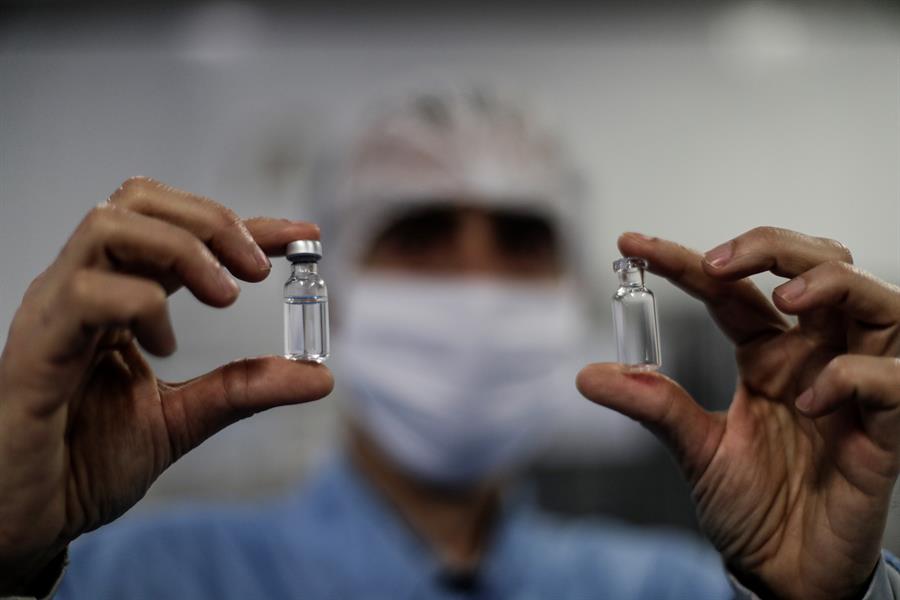
A Agência Nacional de Vigilância Sanitária (Anvisa) anunciou, nesta quarta-feira, 2, os critérios que o órgão utilizará para analisar se autoriza ou não o uso emergencial de vacinas contra a Covid-19. “Para concessão da autorização temporária, a Anvisa analisará caso a caso e a decisão ficará a cargo da Diretoria Colegiada da Agência. Serão considerados dados de estudos não clínicos e clínicos, de qualidade, boas práticas de fabricação, estratégias de monitoramento e controle, resultados provisórios de ensaios clínicos, entre outras evidências científicas. Além disso, a empresa deve apresentar informações que comprovem que a fabricação e a estabilidade são adequadas para garantir a qualidade da vacina”, diz a nota publicada no site da agência reguladora.
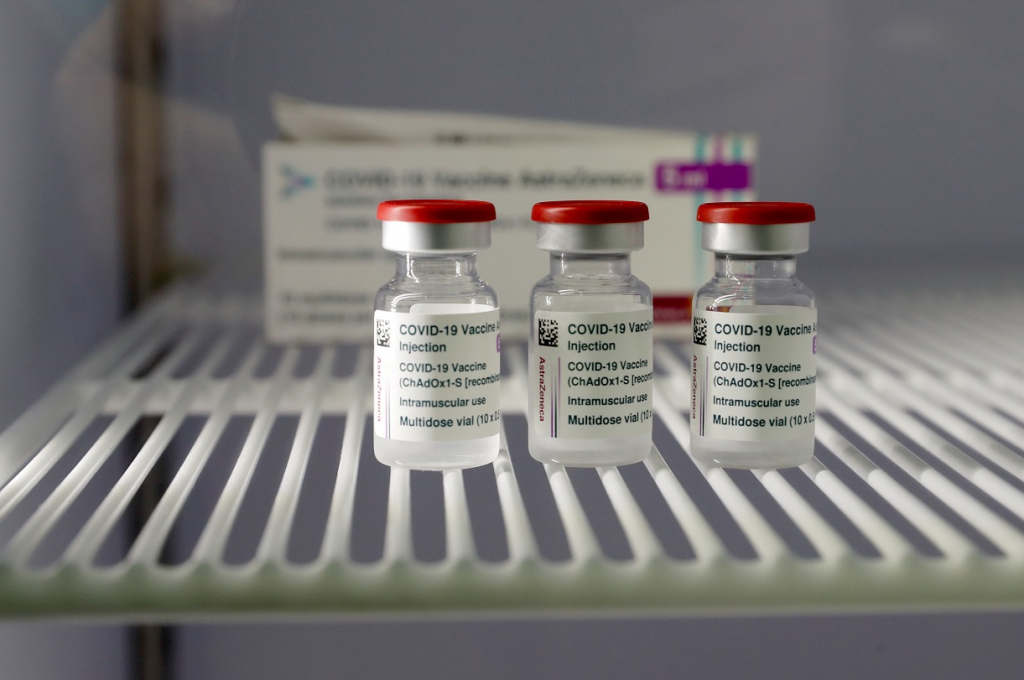
Ainda de acordo com a Anvisa, o pedido de uso emergencial e temporário deve ser submetido pela empresa desenvolvedora da vacina contra o coronavírus. “Antes da submissão formal do pedido de autorização temporária, a empresa requerente deverá agendar uma reunião com a Anvisa, por meio da Gerência Geral de Medicamentos e Produtos Biológicos. A requerente, ao pleitear a autorização temporária, se comprometerá a concluir o desenvolvimento da vacina, apresentar e discutir os resultados com a Anvisa e solicitar seu registro sanitário, desde que atendidos os requerimentos regulatórios, conforme legislação sanitária vigente”, diz outro trecho da nota. Além disso, o ensaio clínico do projeto de imunizante deve estar, pelo menos, na fase 3. No Brasil, estão neste estágio as vacinas desenvolvidas pela Universidade de Oxford em parceria com a farmacêutica AstraZeneca, pelo laboratório chinês Sinovac, em parceria com o Instituto Butantan, pela Johnson & Johnson, e pela Pfizer em parceria com a BioNTech.
Fonte: Jovem Pan