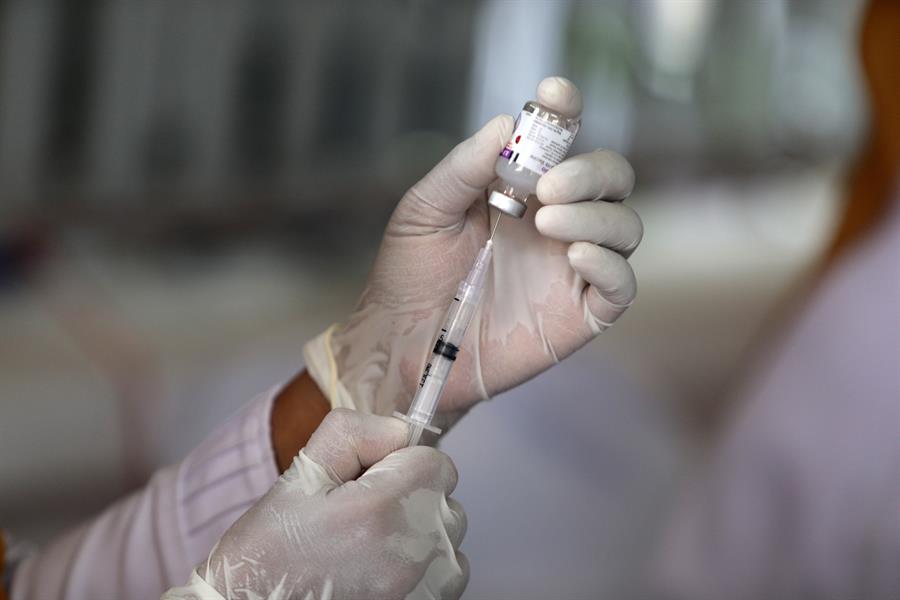
A Agência Nacional de Vigilância Sanitária (Anvisa) definiu critérios para o uso emergencial de vacinas contra a Covid-19. A autorização será temporária e pode ser revista a qualquer momento, caso os testes indiquem que o risco do imunizantes não compensaria o benefício que ela pode trazer. O gerente de medicamentos da Anvisa, Gustavo Mendes, explicou que não há como a agência se comprometer ainda com datas para o início da vacinação, sendo que essas vacinas sem registro não poderão ser comercializadas, apenas utilizadas em campanhas de vacinação do governo federal. Com isso, as clínicas particulares, neste primeiro momento, não terão acesso aos imunizantes. Todas as doses serão direcionadas para o setor público e a previsão é que só seja possível pagar pela vacina da Covid-19 em 2022. A Anvisa espera pela chegada dos primeiros pedidos de autorização emergencial de laboratórios que tiverem estudos na chamada fase 3 de testes, sendo que as etapas devem estar sendo feitas no brasil. A Anvisa vai considerar público alvo, possíveis efeitos colaterais e o procedimento de fabricação na hora da análise. “A autorização de uso emergencial não implica diminuir os critérios e o rigor de qualidade, segurança e eficácia necessários. Ainda existem dados a serem gerados, ainda existem informações a serem compiladas.”
Fonte: Jovem Pan