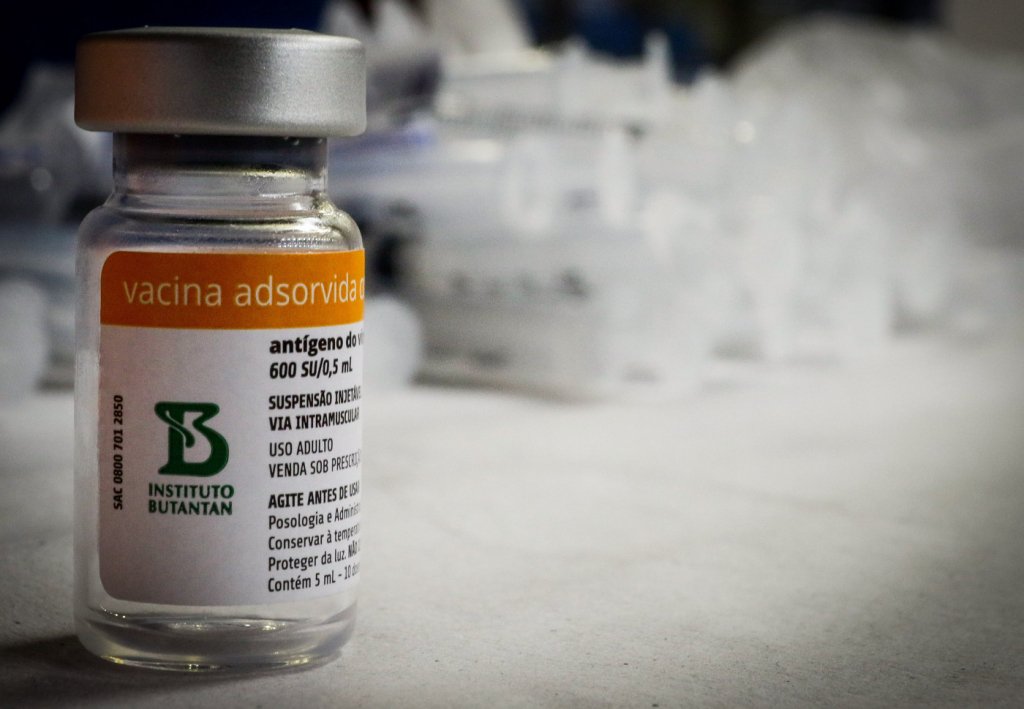
A Agência Nacional de Vigilância Sanitária (Anvisa) recebeu uma notificação sobre um evento adverso grave durante os testes da vacina desenvolvida pela Janssen, divisão farmacêutica da Johnson&Johnson, contra a Covid-19. Segundo a agência, o evento teria acontecido no dia 2 de janeiro com um voluntário brasileiro da fase 3 dos testes para o desenvolvimento do imunizante. Em comunicado, a Anvisa disse que não houve necessidade de suspender os testes clínicos, já que, segundo a farmacêutica, o recrutamento de voluntários foi finalizado no dia 9 de dezembro de 2020. Com isso, não existem mais voluntários que irão receber a vacina teste ou o placebo. A Janssen diz ainda que, “de acordo com o investigador, o evento foi avaliado como não relacionado à vacina”. Em nota, a Anvisa diz que, segundo regulamentos nacionais e internacionais de Boas Práticas Clínicas, informações e dados sobre os voluntários serão mantidos em sigilo para “proteção dos participantes”. A agência também afirmou que não irá informar se o voluntário recebeu a vacina ou o placebo.
Fonte: Jovem Pan