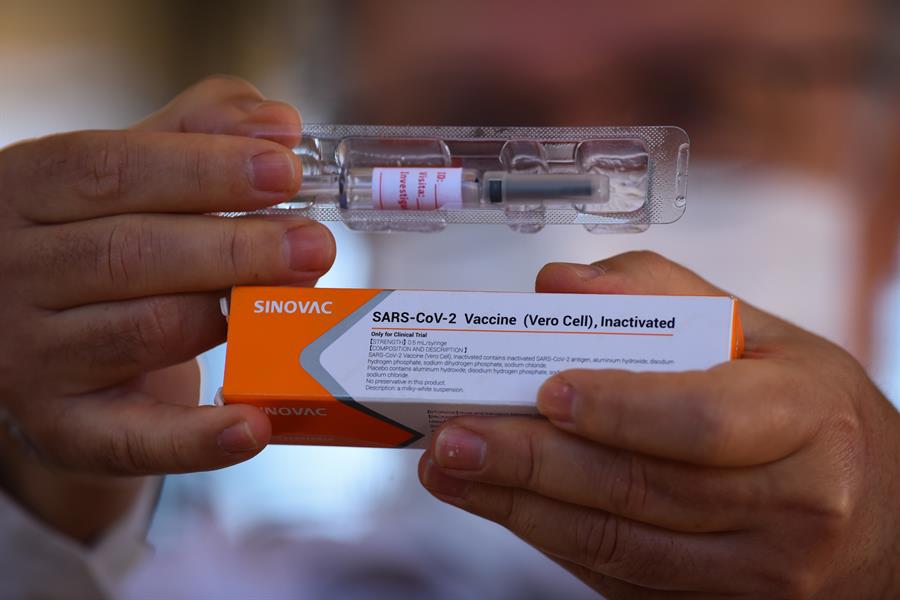
A Agência Nacional de Vigilância Sanitária (Anvisa) concluiu neste sábado,9, a triagem dos documentos enviados pela Fundação Oswaldo Cruz (Fiocruz) e o Instituto Butantan para a liberação do uso emergencial das vacinas contra a Covid-19 produzidas no Brasil por estes laboratórios. O imunizante de Oxford terá a reposta até o próximo dia 18. “O pedido traz os documentos preliminares e essenciais para a avaliação detalhada da agência. A partir de agora, a equipe técnica vai se aprofundar na análise dos dados e informações apresentadas pela Fiocruz”, informou a Anvisa. Já os responsáveis pela CoronaVac precisarão enviar dados que estão faltando, de acordo com o órgão regulador.
“Após a triagem de todos os documentos fornecidos, os técnicos da Anvisa verificaram que ainda faltam dados necessários à avaliação da autorização de uso emergencial. A Anvisa enviou hoje, sábado, 09/01, ofício ao Instituto Butantan solicitando a apresentação dos documentos técnicos faltantes, previstos no Guia 42/2020 (Requisitos para submissão de solicitação de autorização temporária de uso emergencial Vacinas – COVID-19), bem como nos regulamentos técnicos da agência. O recebimento do ofício foi confirmado pelo Butantan às 11h29. A submissão dos documentos técnicos previstos no guia é condição necessária para viabilizar a avaliação, conclusão e a deliberação sobre a autorização de uso emergencial das vacinas.”
Fonte: Jovem Pan