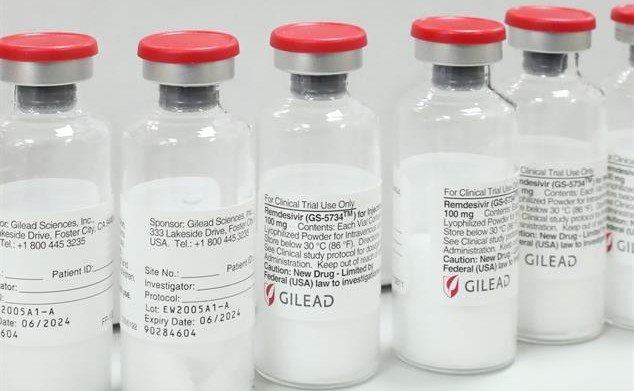
A Agência Nacional de Vigilância Sanitária (Anvisa) aprovou, na manhã desta sexta-feira, 12, o primeiro registro de um medicamento contra Covid-19. O remédio é o Remdesivir, antiviral da Gilead Sciences. Inicialmente, o fármaco foi desenvolvido pela empresa para o tratamento de pacientes com ebola, mas se mostrou ineficaz contra o vírus. Em maio de 2020, a FDA (Food and Drugs Administration), agência federal dos Estados Unidos de controle de alimentos e medicamentos, autorizou o uso emergencial do antiviral em pacientes da Covid-19. Pesquisadores relataram que o remédio reduziu o tempo de recuperação em pessoas que adoeceram com o novo coronavírus. Em julho do mesmo ano, foi a vez da União Europeia autorizar o uso do Remdesivir.
Em outubro, um estudo encabeçado pela Organização Mundial da Saúde (OMS) apontou que o medicamento não surtiu efeito contra o coronavírus. Segundo o Solidarity Therapeutics Trial, o Remdesivir, a hidroxicloroquina, o interferon beta-1a e a combinação de lopinavir e ritonavir são ineficazes. O estudo foi um ensaio randomizado, padrão ouro, com normas rígidas para coleta de evidências científicas. Ao todo, participaram 11.266 adultos em mais de 30 países. Foram relatadas 1.253 mortes durante a pesquisa, e, de acordo com a pesquisa, os medicamentos “desempenharam pouco ou nenhum papel na redução da mortalidade ou tempo de internação pela Covid-19”. Mesmo assim, dias depois da divulgação do estudo, o Remdesivir recebeu a aprovação final para ser utilizado no tratamento da Covid-19 nos EUA. A OMS chegou a desaconselhar o uso em vista do alto custo e possíveis riscos à saúde de um medicamento que deve ser administrado por via intravenosa.
Por que, então, a Anvisa autorizou o uso?
De acordo com a Anvisa, os dados demonstraram que o tratamento com o medicamento pode prevenir uma progressão da Covid-19 em adultos e adolescentes com pneumonia que requerem administração suplementar de oxigênio, através do menor tempo de recuperação e, consequentemente, reduzindo o tempo de hospitalização. “O estudo da OMS avaliou mais a ocorrência de mortalidade e pacientes com perfil um pouco diferente dos avaliados nos outros estudos, que consideramos para liberar o remédio. O estudo que consideramos válido focou na redução do tempo de hospitalização dos pacientes e vimos que houve uma redução na hospitalização. Consideramos que é mais uma terapia para ajudar no combate”, disse Renata Lima Soares, gerente de Avaliação de Segurança e Eficácia.
Em quais outros países o uso do remédio foi aprovado?
O fármaco foi aprovado pela age?ncia Europeia (EMA – European Medicines Agency) e também na Argentina, Austrália, Canada?, Estados Unidos, Emirados A?rabes, Hong Kong, I?ndia, Iraque, Israel, Japa?o, Li?bano, Ru?ssia, Singapura , Coreia do Sul e Sui?c?a.
Quem pode utilizar o Remdesivir?
A dose é recomendada para pacientes com idade igual ou superior a 12 anos e que pesam, pelo menos, 40 kg. O remédio não é recomendado para a forma leve, moderada ou grave da doença. A recomendação está ligada à apresentação de pneumonia com necessidade do suplemento de oxigênio. O paciente, no entanto, ainda não pode estar em ventilação mecânica ou ventilação com membrana extracorpórea. A infectologista e professora da Faculdade de Ciências Médicas da Unicamp, Raquel Stucchi, em entrevista ao Jornal da Manhã, explica que é indicada à administração do medicamento no momento antes do paciente necessitar do respirador.
Como o medicamento deve ser administrado?
O medicamento poderá ser armazenado em temperatura ambiente e sua validade é de 36 meses. Deve ser administrado em uma dose única, de 200 mg, por infusão intravenosa, preparada a partir de um pó. A partir do segundo dia, a dose aplicada deve ser de 100 mg. O tratamento deve ser realizado por no mínimo cinco dias e no máximo 10 dias.
Existem efeitos colaterais?
O u?nico efeito adverso grave relatado em menos de 5% dos participantes em qualquer grupo de tratamento foi insuficie?ncia respirato?ria. Eventos adversos renais foram relatados em 18% do grupo que tomou o medicamento e 23% no grupo que recebeu placebo. Nenhuma morte foi considerada pelos investigadores como relacionados com o tratamento. “A maioria dos eventos adversos estão relacionados a manifestações adjacentes de Covid-19 e não necessariamente ligados à terapia com Remdesivir”, afirma Renata Lima Soares, da Anvisa.
Quais são as inseguranças em relação ao medicamento?
Raquel Stucchi ressalta o fato de que, além de não reduzir a mortalidade, o Remdesivir é um medicamento com um custo muito elevado. “É uma medicação com um custo muito elevado. Então, eu não sei qual será a disponibilidade dela tanto no Sistema Único de Saúde (SUS) quanto nos hospitais privados. A melhora que ele mostrou não é uma melhora tão significante assim, pelo menos nos estudos até agora. Tanto que a OMS, que deve pensar nos protocolos para todos os países, tanto os mais ricos quanto os mais pobres, não recomenda o uso, porque a melhora foi muito pouco importante para quem usou”, explicou Raquel. A infectologista, no entanto, não descartou o fato do Remdesivir ser mais uma arma contra a Covid-19.
O Remdesivir será vendido em farmácias?
Não. O Remdesivir é exclusivo para o uso hospitalar, afirma Raquel. Isso porque o medicamento é administrado por via intravenosa.