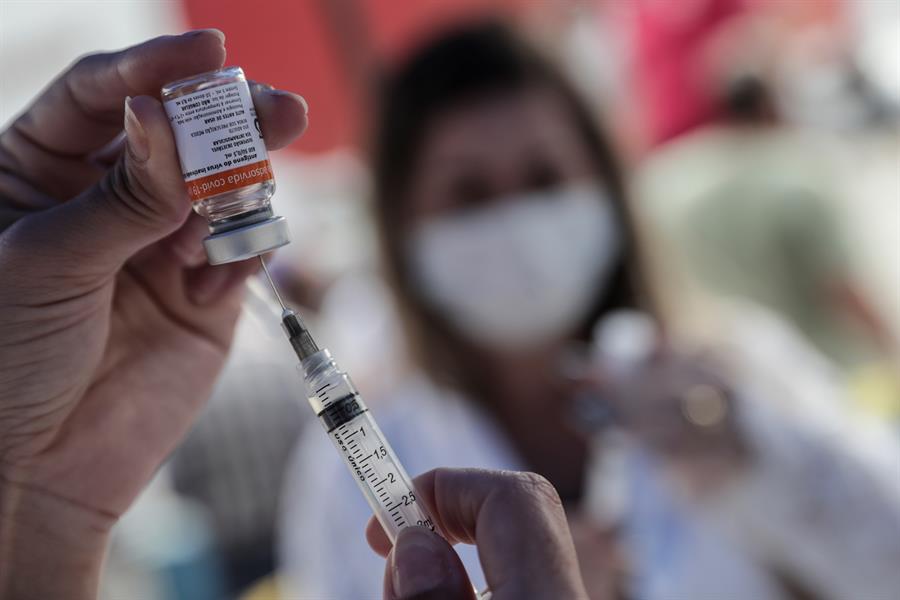
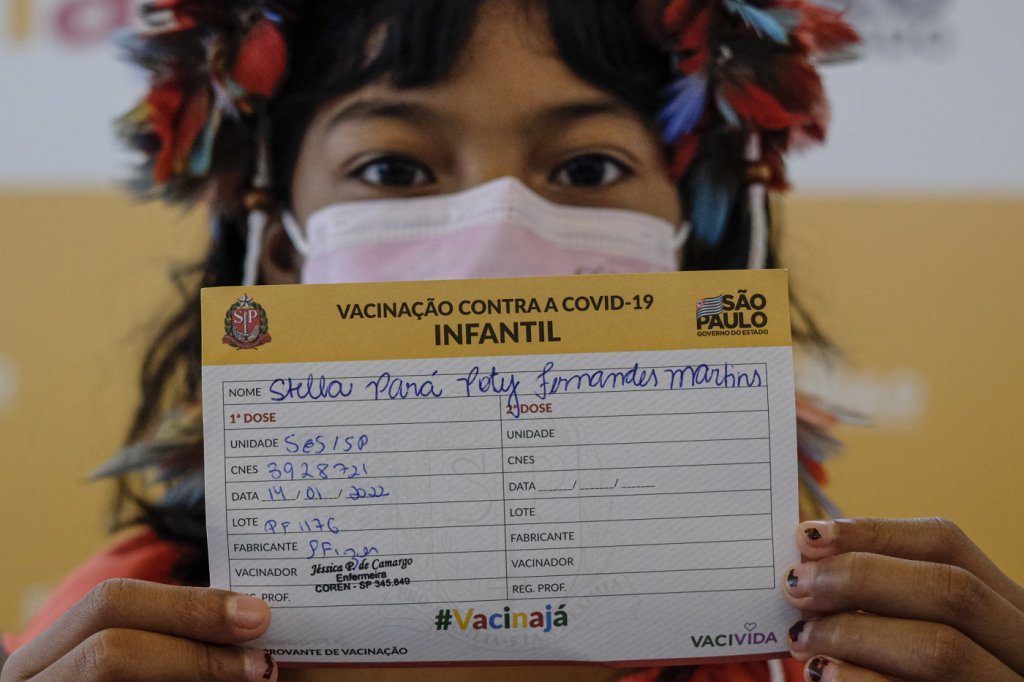
A Agência Nacional de Vigilância Sanitária (Anvisa) anuncia nesta quinta-feira, 17, sua decisão sobre o pedido da Pfizer para utilização do seu imunizante contra a Covid-19 em crianças. A farmacêutica quer expandir a aplicação para a faixa etária de 5 a 11 anos. Estudo realizado pela empresa demonstrou eficácia de 90,7% da vacina contra a forma sintomática da doença. Ao todo, duas mil crianças participaram do estudo, sendo que apenas três das 1.305 que receberam o fármaco desenvolveram a doença, contra 16 das 663 crianças que receberam o placebo. O uso da vacina na população pediátrica foi aprovado pela Agência Europeia de Medicamentos (EMA) em 25 de novembro. A avaliação é que a aprovação ajudaria a acelerar a imunização no continente europeu, que enfrenta novos picos da Covid-19. Além da Europa, os Estados Unidos já utilizam o imunizante da Pfizer na população pediátrica desde o início do mês de novembro.
Ainda sobre a vacinação de crianças contra a Covid-19, o Instituto Butantan entrou nesta quarta-feira, 15, com um pedido para o uso da CoronaVac em crianças e adolescentes de 3 a 17 anos. Essa é a segunda solicitação da entidade para que a faixa etária seja incluída. A primeira foi apresentada em julho à Anvisa e negada por falta de dados sobre o laboratório da Sinovac. Agora, a agência reguladora terá um prazo de 30 dias para análise do pedido. Dimas Covas, presidente do Instituto Butantan, explicou que a CoronaVac é a mais utilizada no mundo. “Só na China são mais de 84 milhões de crianças e adolescentes vacinados. O Chile já vacinando essa população desde setembro, o Equador desde novembro. Então se faz necessário que tenha uma vacina para essa faixa etária e é isso que estamos solicitando”, afirmou.
Fonte: Jovem Pan