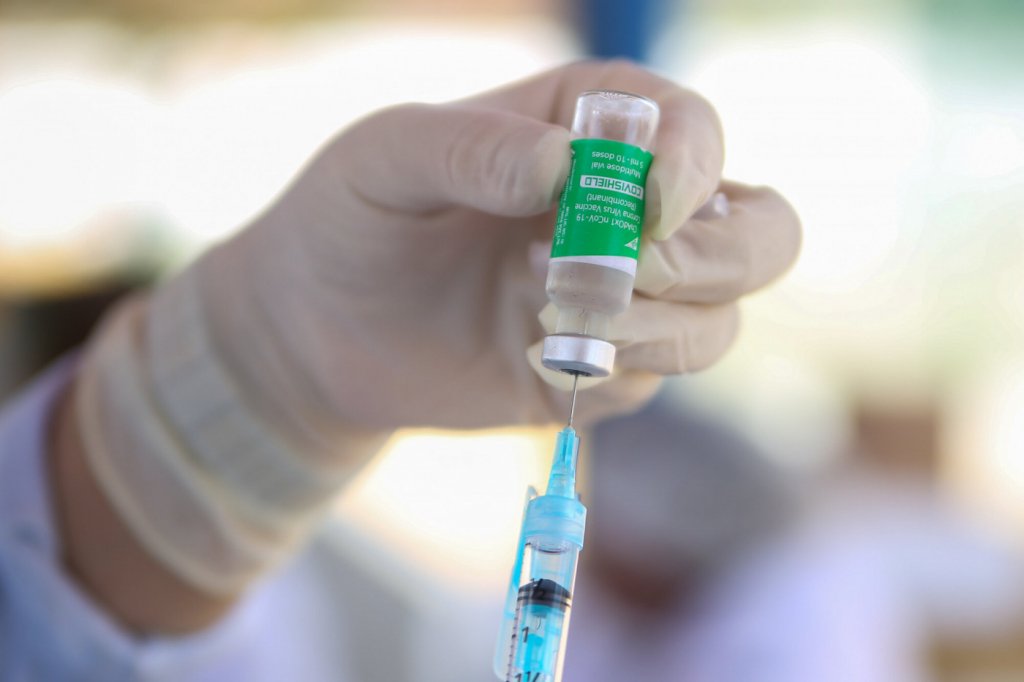
A Agência Nacional de Vigilância Sanitária (Anvisa) aprovou, na manhã desta sexta-feira, 12, o registro definitivo da vacina contra Covid-19 da Universidade de Oxford em parceria com a AstraZeneca no Brasil. No país, o imunizante será produzido pela Fundação Oswaldo Cruz (Fiocruz). O aval permanente da Anvisa é um sinal verde para que o imunizante seja distribuído e utilizado para toda a população prevista na bula — não apenas pelos grupos prioritários permitidos no uso emergencial. A aprovação foi informada pelo gerente-geral de Medicamentos e Produtos Biológicos da Anvisa, Gustavo Mendes. “O dia de hoje é um dia muito importante porque vamos fazer dois anúncios. Dois anúncios de registro que dizem respeito a novas opções que surgem para o enfrentamento da pandemia. O primeiro registro é relacionado à vacina Covid-19 recombinante, mais conhecida como vacina de Oxford, que já vinha sendo usada pelo procedimento de uso emergencial, mas que agora vai ser registrada pela agência com uma etapa de fabricação aqui no Brasil”, explicou Mendes.
A Anvisa também aprovou o primeiro registro de um medicamento contra Covid-19. O remédio é o Remdesivir, antiviral desenvolvido pela Gilead Sciences. O gerente também detalhou o processo da vacina da Janssen, que teve os ensaios clínicos da fase 3 aprovados pela Anvisa. O processo de submissão contínua dos documentos à Anvisa foi iniciado em novembro de 2020. “A Anvisa concluiu a certificação de boas práticas de fabricação das três empresas do processo fabril dessa vacina e, no momento, a gente aguarda a submissão de um pedido de uso emergencial ou de registro definitivo da vacina”, afirmou Mendes. O imunizante da Moderna também está no radar da agência. “A gente não recebeu nenhum pedido de autorização de importação nem autorização de uso emergencial nem de registro desta vacina, porém a gente não vislumbra qualquer barreira ou qualquer critério que a essa vacina possa ter de especificidade que esse imunizante não possa ser solicitado aqui”, explicou. Segundo Mendes, como a Moderna já teve autorização em outros países como Canadá, Estados Unidos e Reino Unido por agências que compartilham do mesmos procedimentos técnicos e regulatórios que a Anvisa.
Fonte: Jovem Pan